2月1日,国际顶级学术期刊《美国化学会志》JACS在线发表了 数字医学工程全国重点实验室/生物科学与医学工程学院吴晓峰、梁高林教授团队的最新研究型论文。论文标题为《可被在体白蛋白截获的近红外光敏剂用于肿瘤靶向耐缺氧光免疫疗法》Caged Ligand-Decorated Near-Infrared Photosensitizer with In Vivo Albumin-Hijacking Capacity for Tumor-Targeted Hypoxia-Tolerant Photoimmunotherapy of Cancer(J. Am. Chem. Soc. 2026, DOI: 10.1002/anie.202416877)。该文章合理设计了酯键修饰的酚类配体,其可被体内白蛋白结构捕获,增强功能性分子瘤内富集。
目前,通过开发人工载体,光敏剂可借助增强EPR效应或主动靶向修饰,有效地递送并积聚于肿瘤组织。然而,多功能载体仍面临严峻挑战,如不确定的长期生物安全性、有限的生物降解性、以及快速清除等问题。相较于人工载体,白蛋白作为一种天然的"隐形"载体,具有较长的循环半衰期,并能通过受体介导的胞吞作用实现内在的肿瘤归巢能力,提供了一种有吸引力的替代方案。然而,现有的白蛋白劫持策略主要依赖体外或通过共价/非共价结合在体内原位构建,存在若干问题,包括:(1) 物理吸附或疏水性结合导致对药物-白蛋白相互作用的控制不足以及脱靶释放;(2) 体外多重合成过程导致的生物活性降低、制备问题以及结果不可重复;(3) 在体内给予治疗剂后与白蛋白相互作用时,可能受到某些物质如蛋白质的干扰。
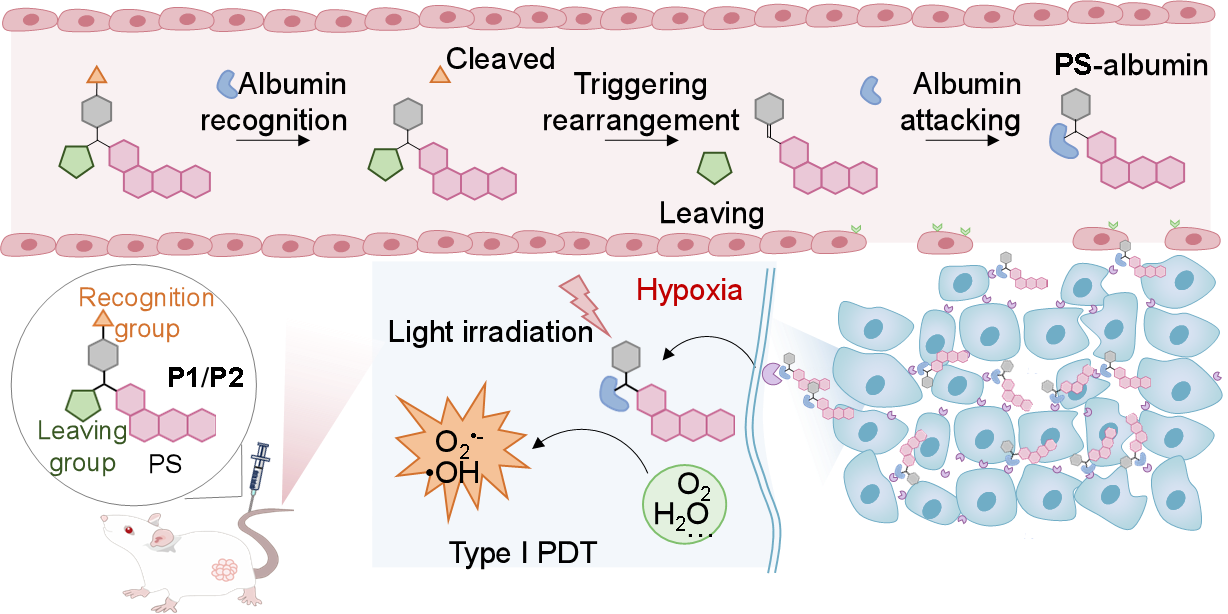
为此,研究团队设计了一种小型配体修饰的耐缺氧I型光敏剂分子(P1),该分子不含传统的靶向基团,表现出优异的肿瘤累积并克服瘤内缺氧以实现增强光免疫疗法。P1主要包含一个由4-羟基扁桃体酸、乙酰基以及离去基团组成的配体,用乙酰基作为白蛋白的识别单元对酚羟基进行,并使用作为离去基团的二茂铁连接苄基羟基,同时还包含一个耐缺氧光敏剂功能单元。与此同时,通过使用乙胺取代P1中的二茂铁,设计了P2作为阳性对照。此外,还设计了两个对照探针,P3具有乙酰基但没有离去基团,P4既没有乙酰基也没有离去基团,作为阴性对照。当与白蛋白相互作用时,P1可以脱去乙酰基,同时伴随1,6-重排消除,形成亚甲基醌(QM)。该QM被白蛋白捕获形成加合物,这一过程可以通过高效液相色谱分析、质谱和吸收光谱得到证实。有趣的是,荧光成像显示,通过尾静脉注射探针后,与P3/P4相比,P1/P2在4T1小鼠肿瘤模型中富集增强。P1进一步也在由HepG2、CT26和ID8细胞系构建的肿瘤模型中实现了很好的肿瘤靶向。在激光照射存在下,P1介导的PDT通过直接消融原发肿瘤实现乳腺癌肿瘤抑制效果(约92%抑制率)。此外,结合PD-L1,光免疫抑制原位和远端肿瘤(抑制率均为95%左右)。这项工作挑战了肿瘤靶向必然依赖配体-受体相互作用的传统范式,不仅提供了一种简单而强大的分子设计,用于肿瘤靶向的非氧原非依赖性PIT药物,还推动了增强药物递送的新范式。
该论文第一作者/通讯作者是 生物科学与医学工程学院的青年首席教授吴晓峰,梨花女子大学的Juyoung Yoon教授、中国地质大学(武汉)胡晶晶副教授与 首席教授/数字医学工程全国重点实验室副主任梁高林为文章的共同通讯作者。 为论文的第一单位。该研究得到了 校启动资金和国家自然科学基金青年基金(C类)、重点项目等的资助。
文章链接:https://pubs.acs.org/doi/10.1021/jacs.5c16988

